Саркоцистоз (саркоспоридиоз) — паразитарное заболевание млекопитающих, птиц и рептилий вызываемое простейшими рода Sarcocystis (саркоцистами) сопровождающееся поражением мышечной ткани и внутренних органов и характеризуется образованием в мышцах цист (мишеровых мешочков).
Саркоцистоз животных распространен повсеместно. Возбудителями саркоцистоза являются паразиты: у крупного рогатого скота S. bovicanis, S. bovifelis и S. bovihominis; у овец – S. ovifelis, S. ovicanis; у свиней – S. suicanis, S. suifelis, S. suihominis. Заражение происходит при заглатывании ооцист вместе с кормом и водой. Основным источником заражения животных являются собаки, кошки, дикие хищники и человек. Плотоядные животные (кошки, собаки) и человек являются дефинитивными (окончательными) хозяевами возбудителя, а травоядные, всеядные животные, грызуны и птицы промежуточными.

Цикл развития саркоцист включает две фазы, протекающие в организмах двух хозяев, принадлежащих различным видам. Половая фаза размножения протекает в кишечнике основного хозяина и завершается образованием ооцист или спороцист, выделяемых с калом основных хозяев. Бесполая фаза происходит в организме промежуточного хозяина: при попадании в пищеварительный тракт ооцист или спороцист происходит высвобождение спорозоитов, которые проникают через стенки желудка или кишечника в кровоток и затем в мышцы, где образуют цисты, заполненные трофозоитами. В организме крупного рогатого скота, овец и свиней паразиты встречаются в виде цист, исключительно в мышечной ткани. Их часто называют «мишеровыми мешочками». Форма цист паразита, в зависимости от места их локализации, может быть веретенообразной, эллипсовидной, неправильной, похожа на зерна риса, размеры — от микроскопических до 2 см.
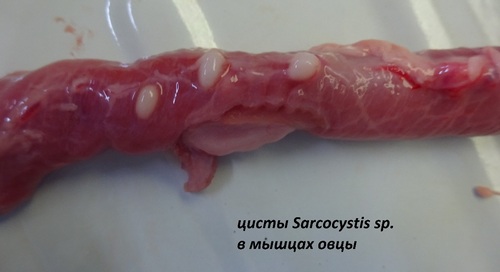
Патогенное влияние саркоцист на организм складывается из их механического и токсического действия. Установлено, что высокая степень распространения заболевания отмечается среди собак. Зараженная саркоцистозом собака способна выделить в сутки около 30 млн. ооцист. Саркоцисты достаточно устойчивы во внешней среде, могут сохранять жизнеспособность более трёх лет, перезимовывать в почве, переносить замораживание и оттаивание, что значительно увеличивает риск распространения заболевания.
Саркоспоридиозы человека зачастую протекают бессимптомно и трудно диагностируются, человек при этом может выступать в роли как основного, так и промежуточного хозяина саркоцист.
Кишечный саркоспоридиоз наблюдается в случае, когда человек выступает в роли основного хозяина и вызывается видами S. hominis, S. suihominis и S. bovihominis. Инфицирование происходит при употреблении не проваренного или не прожаренного мяса свинины, говядины, содержащего саркоцисты. Протекает заболевание обычно бессимптомно, в некоторых случаях сопровождается диспепсическими явлениями, ознобом, лихорадкой. Выделение спороцист с калом начинается на 10-й — 13-й день после инфицирования и может длиться до шести месяцев. Кишечный саркоспоридиоз достаточно широко распространён.
Мышечный саркоспоридиоз возникает при инфицировании спороцистами, когда человек выступает в роли промежуточного хозяина и вызывается S. lindemanni. Инфицирование происходит через загрязненную пищу, руки, бывшие в контакте с болеющими кишечной формой. При проникновении в скелетные мышцы и миокард образуются цисты, которые впоследствии могут обызвествляться. В некоторых случаях сопровождается мышечной болью и общим недомоганием, встречается крайне редко.
У утиных птиц свои виды саркоцист - Sarcocystis rileyi и другие. Важно то, что они не паразитируют у человека. Но употреблять в пищу зараженное саркоцистозом мясо птицы не стоит, так как паразит выделяет токсин - саркоцистин проникающий в мясо. Он не разрушается даже при термической обработке, поэтому может вызвать кишечное расстройство (диарею).
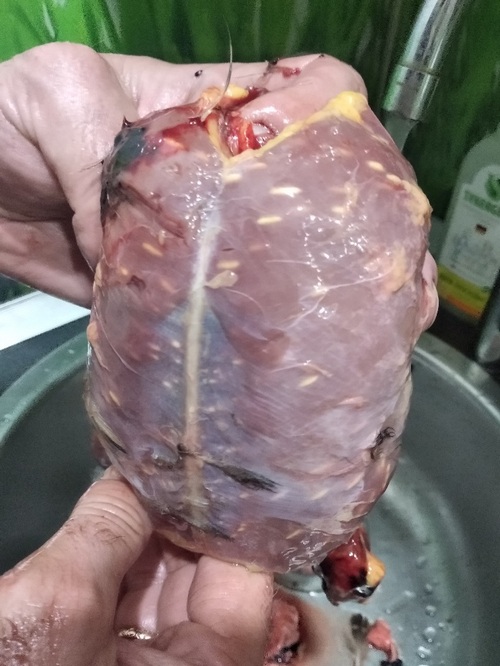

Диагностика: Для установления наличия ооцист и спороцист у собак и других плотоядных животных исследуют фекалии методами флотации.
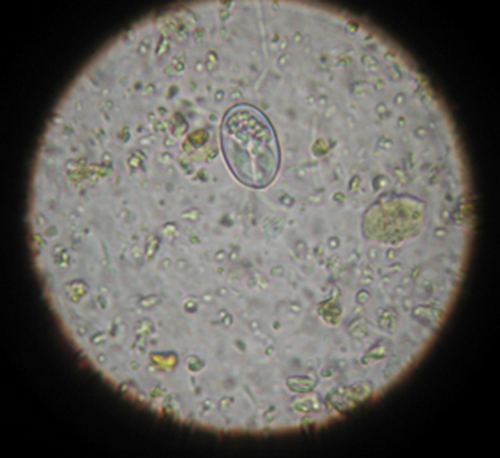
ооциста Sarcocystis sp. в фекалиях собаки.
У жвачных животных саркоцистоз обнаруживают при проведении ветеринарно-санитарной экспертизы, исследуют мышцы диафрагмы, языка, межреберные и жевательные компрессорными методами.
Паразитологическая диагностика у человека. В нативных и постоянных окрашенных препаратах, полученных путем биопсии, или в гистологических срезах из мышц обнаруживаются цисты. Редко цисты могут быть выявлены при рентгенологическом исследовании.
Санитарная оценка мяса при саркоцистозе основывается на степени макроскопических видимых изменений в мышечной ткани, которые могут возникать под влиянием паразитов. При сильном поражении, вызвавшем изменения мышц, туши утилизируют или уничтожают.
Для того, чтобы обеспечить безопасность своего здоровья, следует употреблять в пищу проверенное, хорошо термически обработанное мясо и соблюдать правила личной гигиены после контакта с животными.
Пищевые токсикозы - это заболевания, возникающие при употреблении пищевых продуктов, содержащих токсины бактерий. К этой группе относятся стафилококковые токсикозы, стрептококковые токсикозы, токсикозы, вызванные анаэробными микроорганизмами, микотоксикозы.
Чаще встречаются стафилококковые и стрептококковые токсикозы.
Стафилококки.

Стафилококк был впервые обнаружен в 1878 г. Пастером в гное. В 1881 г стафилококк был получен в чистой культуре; детально изучили его свойства и доказана этиологическая роль в гнойных процессах.
Большинство токсиногенных стафилококков образуют золотистый пигмент.
Еще в XIX столетии была установлена способность отдельных штаммов стафилококков производить токсин. При этом они обладают большой гемолитической способностью, разрушая эритроциты различных животных, особенно кроликов, лейколитической активность, сначала изменяя, а затем растворяя лейкоциты. Проявляют дермонекротическую способность при внутрикожном введении, особенно в отношении кроликов и при внутривенном введении вызывает смертельную токсемию. Стафилококковые токсины по типу являются экзотоксинами и обладают антигенными свойствами. Они образуются патогенными видами стафилококков, чаще золотистым.
Стафилококк поражает у человека кожные покровы, вызывая фурункулез, карбункулез, импетиго, абсцессы, гнойные флегмоны, нагноение ран и т.д.
Кроме того, стафилококк является возбудителем маститов, остеомиелитов, гнойных артритов, пиелонефритов, абсцессов печени, бронхов и т.д. При попадании стафилококка в кровь возникает общая пиемия.
В патологии животных стафилококки играют не меньшую роль, чем в патологии человека, вызывая местные воспалительные процессы, так и общие заболевания.
Роль некоторых видов стафилококков в пищевых отравлениях впервые наблюдал в 1901 г Пащенков. Который описал случай пищевого отравления в Харькове, после употребления кремовых тортов, приобретенных в одной и той же кондитерской. Из крема был выделен золотистый стафилококк. В 1906 г русский бактериолог Яковлев описал вспышку отравлений с указанием на стафилококковое происхождение этого заболевания.
Признаки стафилококковых отравлений по данным Игнатович, основанном на многолетних наблюдениях обычно возникало через 2-5 ч (редко через 1-6ч) после приема пищи с симптомами: головная боль, головокружение, общая слабость, понос, тошнота, рвота с судорожными позывами, боли в подложечной области; в тяжелых случаях – упадок сил, сердечной деятельности, иногда цианоз, ослабление зрения, потеря сознания с падением кровяного давления. Выздоровление через 1-3 суток; смертельные случаи крайне редко.
Анализ пищевых отравлений, вызванных стафилококком, показывает, что основой заболеваний лежит токсическое начало, т.е восприятие с пищей готовых энтеротоксинов.
С точки зрения пищевых отравлений факт обнаружения стафилококков в пищевых продуктах сам по себе ещё ничего не говорит т.к. далеко не все штаммы стафилококков обладают энтеротоксическим свойством. Стафилококковые отравления обусловлены возможностью того или иного штамма продуцировать в определенных условиях энтеротоксин.
На способность токсинообразования стафилококков оказывают большое влияние питательная среда и температурные условия. Среда с большим содержанием белка и крахмала благоприятно влияет на размножение стафилококков и на токсинообразование. Этим объясняется, частые отравления после употребления в пищу молока и кондитерских кремовых изделий, представляющие хорошую среду для токсинообразования. Факт, что энтеротоксины могут разрушаться в молоке при сыроварении и сохраняться при созревании сыра, объясняет описанные в литературе случаи стафилококкового отравления сыром.
Источниками стафилококковых отравлений могут служить рыба и рыбные продукты. К.И. Туржецкий(1949 г) впервые описал вспышки отравлений при употреблении рыбы и рыбных консервов в масле (копченая треска, шпроты, корюшка в масле). Это объясняется тем, что при плохой теплопроводимости масла и значительной теплоустойчивости некоторых штаммов стафилококков стерилизация не всегда приводит к разрушению токсинов и гибели микроорганизмов. По исследованиям Н.П. Нефедьевой (1955г) стерилизация рыбных консервов в масле при температуре 112 °C не всегда разрушает энтеротоксин; стерилизация при 120 °C полностью разрушает токсин.
А содержание в продукте до 12% соли не препятствует размножению стафилококков и токсинообразованию. Ф.Л. Вильштанская и М.И.Гершейн (1955 г) наблюдали вспышку отравлений при употреблении в пищу селедки.
Работы Бамм, Рекстень показали, что в молоке, креме, брынзе и смеси для мороженного токсины могут образовываться при температуре 15-22°C через 12-20 ч. По данным Бамм, при 8-10°C размножение стафилококков и токсинообразование идет медленно, при переносе в благоприятные условия этот процесс набирает скорость.
Энтеротоксин устойчив к высоким температурам. На холоде, при температуре ледника и при комнатной температуре, энтеротоксины сохраняют свою активность до нескольких недель.
Источники инфицирования пищевых продуктов это животные, страдающие маститом, а также человек, который может носить эти микробы в самых разных органах (в носу, в зеве, в гортани), но особенно на руках, при гнойничковых поражениях кожи.
По сообщениям Орлова, стафилококковые токсикозы могут протекать не в виде желудочно-кишечного заболевания, а при картине «алиментарной ангины».
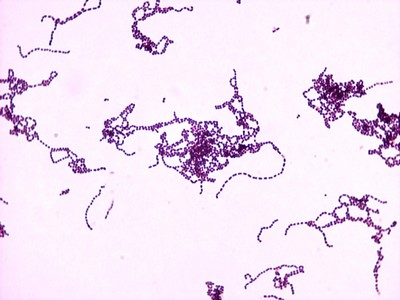
Стрептококки.
Стрептококки представляют собой весьма обширную гетерогенную группу микробов. Патогенные стрептококки вызывают у людей и животных различные заболевания.
У людей стрептококки бывают причиной таких заболеваний как рожа, стрептодермия, эндокардит, послеродовая септицемия, смешанные стептококовая и стафилококковая инфекции, скарлатина. Аристовский, Минкевич, Фрид указывают, что наличие в молоке гемолитических стрептококков неоднократно приводило к вспышке тяжелых заболеваний алиментарной ангины.
У животных стрептококки могут вызывать такие первичные инфекции как мыт и инфекционный мастит. В качестве вторичных возбудителей они обнаруживаются при бронхопневмонии. Могут вызывать у животных абсцессы, флегмоны, экземы, флебиты и т.д.
Из лабораторных животных к стрептококкам восприимчивы мыши, кролики, в меньшей степени морские свинки. Путем пассажа через животных удается повысить вирулентность стрептококков к тому виду животных, через который стрептококки пассажируются.
В 1931и 1938 г в США описаны три вспышки пищевых токсикоинфекций, обусловленные Str. viridans (по американской номенклатуре L- стрептококки). В первом случае заболевания, возникли после употребления сосисок в консервных банках, не подвергшихся тепловой обработке, начались через 4-5 ч после еды при явлениях тошноты, рвоты, поноса, болей в животе, и закончились через сутки. Из оставшихся неиспользованными сосисок был выделен Str. Viridans. Один из сотрудников лаборатории, выпивший 40 мл пятидневной бульонной культуры выделенного стрептококка, заболел через 5 ч с описанными признаками. Другой сотрудник, выпивший 50 мл. фильтрата бульонной культуры, не проявлял никаких признаков заболевания. Мыши, кролики, морские свинки и обезьяны, получившие per os выделенные культуры, не обнаружили никакой реакции. Однако у котят, при пероральном введении им молочной культуры стрептококка, наблюдались признаки энтерита.
Вторая вспышка возникла после употребления в пищу мясных фрикаделек. Из 208 человек, употребляющих это блюдо, заболело 117 с признаками поноса, тошноты, рвоты, и болей в животе. Инкубационный период длился 6-18, в среднем 12 часов. Из фрикаделек был выделен Str. Viridans. Семь добровольцев, выпивших с молоком 20 мл. фильтрата стрептококковых культур, не обнаружили признаков заболевания. При приеме же живых бульонных культур у пяти развились желудочно-кишечные заболевания.
Третья вспышка возникла после употребления в пищу фаршированных индеек. Заболевание начались через 8-12ч после приема пищи, с явлениями тошноты, поноса, болей в животе. Из неиспользованной пищи выделен Str. Viridans.
С эпидемиологической точки зрения приобретает большое значение вопрос о том, являются ли пищевые отравления, вызываемые стрептококками, чистыми токсикозами, обусловленными энтеротоксинами, или токсикоинфекциями, связанные с участием самих микроорганизмов. Например, по данным Педенко, Лерина, Белицкого стрептококки — это условно-патогенная микрофлора, вызывающая токсикоинфекции. К ним относятся зеленеющий стрептококк и фекальные энтерококки.
Известно, что различные виды стрептококков могут образовывать ядовитые вещества типа экзотоксинов, обнаруживаемые в фильтратах культур и обладающие гемолитической, лейколитической и фибролотичиеской активностью.
Черкасова детально изучала токсигенные свойства септического диплококка (Dipl. septicus, s. lancelatus), являющегося возбудителем диплококковой септицемии у молодняка, а также маститов и эндометритов у взрослых коров.
Чепуров, изучая изменчивость типичных гемолитических стрептококков, выделенных при эндометритах у коров (Str. mastitidis), обнаружил, что после четырехкратного проведения через мышей эти стрептококки приобретали морфологические признаки диплококков. Для доказательства перехода стрептококка в диплококк автор заразил внутривенно теленка типичным стрептококком, выделенным при мастите у коровы. Теленок вскоре заболел суставной формой диплококковой инфекции. Из синовии суставов этого теленка, убитого на 14 й день заболевания, была выделена типичная культура Dipl. septicus.Чепуров сделал вывод, что основным источником диплококковой инфекции у молодняка являются коровы, страдающие маститом, обусловленным Str. mastitidis, особенно если молодняку скармливают молоко таких коров.
Черкасова установила, что пероральное введении котятам 20-25 мл. фильтрата бульонных культур Dipl. Septicus вызывает у них тяжелое заболевание и смерть (у 28,5 %). Пероральное введение фильтрата в концентрированном (выпариванием) виде увеличивает процент смертности до 66,6 %. Пероральное введение фильтрата Dipl. septicus мышам не вызывает у них заболевание.
Токсические вещества, выработанные Dip. Septicus весьма термоустойчивы вызывая заболевание и гибель котят при пероральном введении даже после кипячения в течение часа. После двухчасового кипячения фильтраты теряют свою токсичность.
При испытании возможности обезвреживания мяса, обильно осемененного Dipl. septicus, Черкасова установила, что проварка такого мяса в течение часа в открытом котле кусками весом в 2 кг и толщиной в 10 см приводит к инактивации микробов. Однако токсичность мяса сохраняется, и скармливание его котятам вызывает тяжелое заболевание. Только при двухчасовой проварке в открытых котлах или при автоклавировании при давлении 1,5 атмосферы мясо теряет свою токсичность и скармливание не вызывает заболеваний котят.
При изготовлении вареных колбас из мясного фарша, обильно обсемененного Dipl. septicus, оказалось, что варка батонов колбасы толщиной в 5 см. при температуре до 85-90°С в течение 1-11/2часов приводит к инактивации диплококков. Однако токсичность колбасы сохраняется, и скармливание её котятам вызывает тяжелое заболевание. Жарение в течение 20-25 минут котлет, приготовленных из фарша, осемененного Dipl. septicus, инактивирует микробов, но и при этом токсичность продукта сохраняется, вызывая заболевание при скармливании.
Источниками пищевых отравлений стрептококкового происхождения могут являться взрослые животные, страдающие маститом и дающие загрязненное молоко стрептококками, а также спадающий диплококковой септицемией молодняк, в мясе которого содержаться живые диплострептококки или вырабатываемый ими энтеротоксин. Носителем является и человек (гнойничковые поражения кожи, наличие стрептококковых заболеваний верхних дыхательных путей), от которого микробы могут попасть в пищевые продукты.
Санитарная оценка продуктов, загрязненной кокковой микрофлорой.
При выделении из глубоких слоев мышц или лимфатических узлов стафилококков или стрептококков внутренние органы бракуют, а мясо выпускают после проварки. Так же поступают с мясом телят при диплококковой септицемии.
По ветеринарному законодательству при обнаружении в глубоких слоях мускулатуры кокковой микрофлоры, а также гнилостных микробов, в особенности протея, но при хорошей органолептической оценке, мясо подвергается тепловой обработке.
В пробах мороженного и оттаянного мяса кокковые формы могут быть засеяны с поверхности в глубокие слои мяса, вследствие движения тканевых жидкостей. Выделенные культуры кокков необходимо исследовать на патогенность и токсичность (путем определения гемолитической активности, способности культур продуцировать фосфатазу и коагулазу, а также биопробой на лабораторных животных). Если выделенные штаммы окажутся токсгенными, то мясо проваривают; если культуры буде тут отнесены к нетоксичным сапрофитам, то мясо выпускают свободно в быструю реализацию (при условии отсутствия органолептических признаков несвежести).
Готовые продукты, из которых выделены токсигенные стрептококки и стафилококки, направляют в техническую утилизацию.
Что касается немясных продуктов, то основные принципы санитарной оценки остаются теми же. Однако здесь особенно большое значение приобретает вид продукта, сточки зрения возможности быстрого развития в нем микрофлоры. Необходимо учитывать, что продукты, содержащие, кроме белка, большое количество углеводов (сладкая среда), являются благоприятной средой для развития в ней микрофлоры и токсинообразования, особенно стафилококков. Отмечено что при наличии ванили или ванилина в молочных продуктах создает благоприятные условия для развития стафилококков в этих продуктах.
При использовании тепловой обработки следует учитывать группу стафилококка, отдельные виды которых способны вырабатывать теплоустойчивые специфические энтеротоксины.
Одним из важнейших показателей качества продукции, определяющим ее пищевую ценность, является содержания белка. Классическим способом определения белка является метод, разработанный еще в 1883 году датским химиком Иоганном Кьельдалем, который впоследствии был назван его именем.
Это очень трудоемкий и продолжительный анализ, и потому в современной лабораторной практике метод Кьельдаля часто пытаются заменить альтернативными методами определения протеина, в том числе, с использованием дорогостоящих программно-аппаратных комплексов. Но метод Кьельдаля, несмотря на его сложность, до сих пор остается единственным общепризнанным арбитражным методом определения протеина, и чаще всего используется в качестве эталонного для калибровки и настройки других методик анализа сырья и готовой продукции.
Сырой протеин – это первый показатель, на который обращают внимание при оценке качества кормов. Стоимость рыбной муки, шротов и некоторого другого сырья зависит от содержания в нем белка.
При анализе питательности полнорационных комбикормов часто смотрят на протеин в первую очередь. Содержание сырого протеина в кормах растительного и животного происхождения, и в комбикормовом сырье можно проверить в нашей лаборатории.
Как известно, питательность корма нельзя выразить одним показателем, она должна быть комплексной. Слово «протеин» происходит от греческого «protos» – «первый». И действительно, это вещество занимает первостепенное значение в кормлении животных, так как его нельзя заменить другими. В биохимии протеином называют простые белки, состоящие только из аминокислот. В кормлении животных под сырым протеином понимают все азотсодержащие вещества корма: белки и амиды.
Значение протеина для животных:
Протеин играет первостепенную роль в построении тела и жизнедеятельности животного организма. Условно можно выделить три основные функции протеина: строительную, биологическую и энергетическую. Строительная, или пластическая, функция заключается в том, что протеин является строительным материалом для синтеза белков организма, входящих в состав всех органов и тканей, являющихся составной частью продукции: молока, мяса, яиц, шерсти.
Дефицит протеина в рационах животных ведет к тяжелым последствиям: снижается продуктивность, ухудшается качество продукции (например, уменьшается в молоке содержание белка и жира), замедляется рост молодняка, возрастает продолжительность выращивания и откорма. Нежелателен и избыток протеина. Во-первых, перерасход протеина не оправдан экономически, во-вторых, избыток протеина также отрицательно сказывается на состоянии здоровья, воспроизводства, долголетии, ведет к снижению усвоения витаминов А, С, группы В.
Для определения сырого протеина в кормах используется метод Кьельдаля. По этому методу определяется общий азот.
Исследование проводится по ГОСТ 13496.4-93.
Метод включает в себя несколько основных этапов: отбор и подготовку проб, мокрое озоление, отгонку и определение концентрации азота (титриметрически) и расчёт содержания сырого протеина.
Этап 1. Отбор и подготовка проб. Необходимое условие получения точных результатов анализа по методу Кьельдаля - тщательная подготовка образцов. Процедура подготовки проб должна обеспечивать гомогенизацию образца. Взвешивание образцов для последующего анализа по методу Къельдаля должно проводиться на аналитических весах с точностью до 0,01 мг.
Этап 2. Мокрое озоление. Самым трудоемким и продолжительным этапом в методе Кьельдаля является стадия мокрого озоления, в результате которого происходит полное "сжигание" образца в чистой серной кислоте в течении 5-6 часов. Скорость озоления и разрушения образца зависят не только от свойств кислоты, но и от температуры обработки. Скорость мокрого озоления значительно увеличить за счет добавления солей и катализаторов.

Этап 3. Отгонка. Полученный после стадии разложения прозрачный раствор не годится для непосредственного определения в нем аммонийного азота из большого содержания мешающих компонентов. Для определения азота из пробирки раствор количественно переносится в отгонную колбу, пробирка обмывается водой. Колба переносится на плитку, добавляется раствор щелочи и отгоняется на установке Кьельдаля для определения аммонийного азота. Раствор отгоняется в приемную колбу с раствором борной кислоты, в которую добавлен индикатор, до изменения окраски раствора с фиолетового до зеленого.



Этап 4. Титрование. Титрование ведется из бюретки раствором серной кислоты определённой концентрации, до перехода окраски раствора от зеленого цвета в фиолетовый. 


Этап 5. Обработка результатов. Вычисляется массовая доля азота и расчет содержания сырого протеина. Расчёт производится по формулам, указанным в ГОСТе.
Несмотря на кажущуюся сложность комплекса оборудования для определения белка по Кьельдалю, использование именно этого метода анализа гарантирует достоверность результатов.
Это природно-очаговое инвазионное заболевание, опасное для человека. Трихинеллез у людей протекает очень тяжело, плохо поддается лечению, часто оканчивается инвалидностью или смертельным исходом.
Возбудитель нематоды рода Trichinella. В природе существует 4 вида трихинелл: T. spiralis, T. nativa, T. nelson, T. pseudospiralis. Это мелкие гельминты, имеют округлое тело и зауженные концы, размеры варьируют от 1,2мм до 4 мм. Самки вдвое длиннее самцов, живородящие. Эти паразитические черви встречаются по всему земному шару, кроме Австралии, но чаще всего болезнь (трихинеллез) диагностируется в северном полушарии.
Как можно заразиться?
Резервуаром инвазии и источником паразитоза для человека в природных очагах являются дикие животные - кабаны, барсуки, медведи бурые и белые, лиса, нутрия, морские млекопитающие – киты, тюлени и др., а в населенных пунктах домашние животные - свиньи, собаки, кошки и др.
Животные заражаются при поедании трупов инвазированных крыс, диких животных, а также сырых боенских и кухонных мясных отходов.
Паразит может попасть в организм человека из-за употребления сырого, недоваренного или недожаренного мяса всеядных и плотоядных животных, содержащего личинки трихинелл.
В группе риска находятся охотники, особенно любители шашлыка из мяса кабана, медведя. Факторами передачи могут быть свиные колбасы, шпик домашнего приготовления, окорок, бекон, грудинка и прочее.
Восприимчивость к трихинеллезу достаточно высока. Достаточно около 10 гр. зараженного мяса для начала инвазии. Нередко заболевают целыми группами или семьями после застолья, охотничьей трапезы.
Сезонность для трихинеллеза чаще осеннее-зимняя (при задействовании природного очага, период охоты), в городских очагах – осень (забой свиней).
Мышечные трихинеллы очень устойчивы к неблагоприятным условиям внешних факторов: в гниющем мясе они сохраняются в течение 4 месяцев. При слабом солении и копчении мяса личинки не погибают. Обычная тепловая обработка не гарантирует 100%-ного обезвреживания мяса, инкапсулированные личинки погибают при тепловой обработке мяса не менее 80ºС внутри куска в течение порядка 4 часов.
Цикл развития.
Один и тот же организм является для трихинелл и основным, и промежуточным хозяином. После того как человек съедает мясо больного животного, плохо термически обработанное, личинки в желудке выходят из капсул и через некоторое время проникают в тонкий кишечник. Примерно через 24 часа молодые особи становятся самками или самцами, которые прикрепляются к стенке кишечника и начинают размножатся. 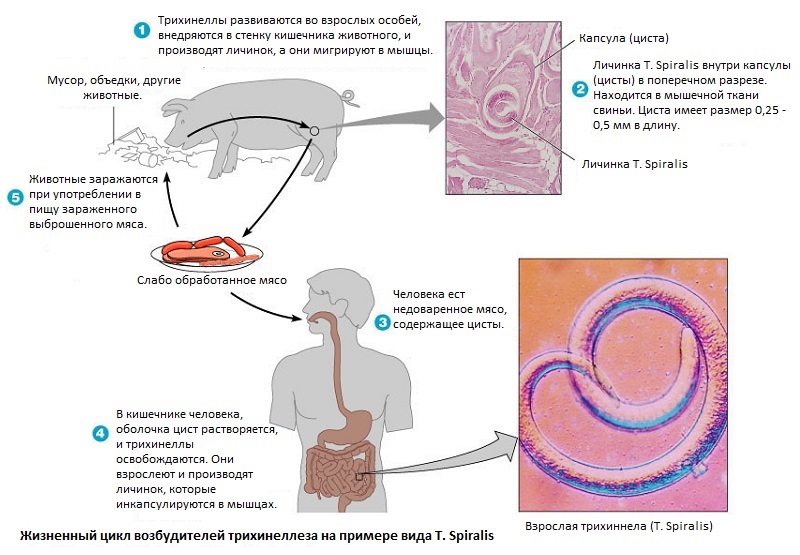
На 4-е сутки после заражения самки отрождают живые личинки. Одна самка способна выделять до 2100 личинок. Период этот длится не больше 2 месяцев. Через слизистую оболочку кишечника они проникают в лимфатическую систему, затем в кровь и разносятся по всему организму.
Через 5-8 дней после заражения личинки попадают в скелетную поперечно-полосатую мускулатуру (практически всех органов, кроме сердца) - чаще языка, предплечья, диафрагмы, межреберных, дельтовидных, икроножных мышц. Далее они инкапсулируются (функции капсулы - питательная, защитная).
Через 6 месяцев начинается обызвествление капсулы, которое продолжается около 2х лет. На данном этапе развитие гельминта заканчивается. В капсулах личинки сохраняют жизнеспособность в течение 25 и более лет.
Как проявляется трихинеллез?
Инкубационный период (период с момента инфицирования до появления первых симптомов заболевания) составляет 10 - 25 дней, но может укорачиваться до недели (при массивных инвазиях) и удлиняться до 45 дней (при легких формах).
При попадании небольшого количества личинок трихинелл высока вероятность того, что человек не обратит внимания на изменения в самочувствии. Но по мере роста (первые 2 недели) могут начать проявляться симптомы: расстройство пищеварения; болевые ощущения в животе; усталость; могут появиться рвота и тошнота.
Но чаще всего люди даже не подозревают, что все эти признаки могут сигнализировать о наличии паразитов, больше склоняются к отравлениям, заболеваниям ЖКТ, поэтому вовремя не предпринимаются нужные меры.
Уже к концу первой недели сформировавшиеся взрослые трихинеллы начинают отрождать юных личинок, которые через лимфу и кровь мигрируют в поперечно-полосатую мускулатуру. Как только личинки достигнут мышечных волокон заболевание проявит себя обязательно. Но от количества паразитов будет зависеть насколько сильно.
Возможны такие симптомы: высокая температура; мышечные боли и слабость; отечность лица и глаз; чувствительность к свету; постоянные инфекции глаз; необъяснимые высыпания на коже; головные боли; озноб.
Общая продолжительность болезни в среднем составляет от 1-2 недель (легкие формы) до 5-6 недель.
Без специального лечения большинство симптомов проходит через 3-4 недели – когда взрослая самка перестает производить на свет новых личинок и гибнет.
При тяжелой форме трихинеллеза период выздоровления может затянуться до 6 и более месяцев.
При этом поражаются: сердце, легкие, мозг. Проявляется расстройством пищеварения, расстройством центральной нервной системы, темными кровоизлияниями под кожу, скованностью в суставах в сочетании с мышечной болью.
Личинки трихинелл поселяются и инкапсулируются в поперечнополосатых мышечных тканях. Зависимо от локализации этих капсул зависят возможные осложнения: Миокардит, энцефалит, менингит, бронхопневмония, нефрит, синусит.
В отсутствии лечения может развиться поражение жизненно-важных органов и возможен летальный исход. Летальность при трихинеллезе может достигать 5%. Однако не всегда легкие формы можно правильно диагностировать и вовремя назначить терапию.
Лечение.
Лечение больных со всеми формами трихинеллеза, кроме стертых, проводят в стационаре, поскольку возможны прогрессирование болезни и тяжелые побочные реакции на специфическое лечение.
После того, как трихинеллез был подтвержден – стоит немедленно начать прием противопаразитарных препаратов, таких как Альбендазол или Мебендазол. Быстрое начало лечения может помочь убить взрослых червей и тем самым остановить дальнейшее появление личинок. После того, как личинки основалась в мышечных тканях (обычно это от 3 до 4 недель после заражения), лечение уже не сможет полностью избавить от инфекции или симптомов. В мышцах они могут находится десятки лет, образовывая вокруг себя специальную капсулу.
Профилактика
По действующему в нашей стране ветеринарному законодательству обязательной трихинеллоскопии подвергается мясо свиней, кабанов, медведей и барсуков и т.д. Исследованию подвергаются мясопродукты независимо от технологии их обработки, т. е. солонина, копченая свинина, в некоторых случаях и колбасы. В случае обнаружения хотя бы одной трихинеллы в 96 мышечных срезах мясо уничтожается сжиганием или отправляется на техническую утилизацию. Поступившие в реализацию мясо и мясопродукты в магазинах и рынках проходят трихинеллоскопию и не представляют опасности. Как правило, заболевания трихинеллезом возникают вследствие использования мяса свиней, забитых в домашних условиях, кабанов, медведей, добытых на охоте и не проверенных лабораторно.
Личная профилактика трихинеллеза состоит в том, чтобы употреблять в пищу только обследованное на трихинеллез мясо свиней и диких животных. Нельзя покупать мясо этих животных или мясопродукты на случайных рынках при отсутствии справки ветсанэкспертизы. Существующие методы соления, копчения мяса не гарантируют уничтожения мышечных трихинелл в глубоких слоях.
Одним из основных продуктов животноводства является молоко, которое представляет собой сложную биологическую жидкость, образующуюся в молочной железе самок млекопитающих. Молоко обладает высокой пищевой ценностью, иммунологическими и бактерицидными свойствами.

Оно является незаменимой полноценной пищей для новорожденных и высокоценным продуктом питания человека всех возрастов. Высокая пищевая ценность молока состоит в том, что оно содержит белки, жиры, углеводы, витамины, ферменты, гормоны, минеральные и другие вещества, необходимые для человеческого организма в оптимально сбалансированных соотношениях и легкоусвояемой форме. Поэтому одной из важнейших задач молочного скотоводства является увеличение объемов производства молока, и самое главное - повышение его биологической ценности и санитарного качества. Последнее, в свою очередь, влияет на здоровье человека, экономический потенциал хозяйств и предприятий молочной промышленности. На качество получаемого молока оказывает влияние санитарное состояние ферм, наличие коров, больных маститом и эндометритом, состояние технологии первичной переработки и хранения. Концентрация на современных комплексах большого количества коров на ограниченных территориях, введение технологии комплексной механизации основных животноводческих процессов сопровождаются ростом заболеваний, особенно молочной железы. Ежегодно у 20-25% коров регистрируется клинически выраженные маститы и у 50% и более животных воспаление, протекающее в скрытой форме. В результате от каждой коровы недополучают около 10-15% молока, снижается содержание в нем жира и белка. Кроме того, из-за болезней молочной железы ежегодно выбраковывается 10% и более высокопродуктивных животных. Борьба с маститами представляет актуальную хозяйственно-экономическую проблему для многих стран с интенсивным молочным скотоводством.
Получение молока с высоким санитарным качеством во многом зависит от зоотехнической и ветеринарной служб хозяйств, специалистов, которые проводят диагностические, профилактические и лечебные мероприятия по ликвидации маститов у коров. Предрасполагающих факторов и причин, вызывающих маститы, много и учесть их все затруднительно. Среди способствующих факторов большое место занимают кормление, содержание животных и так называемые технологические показатели вымени, такие как форма молочной железы, длина и диаметр сосков, продолжительность доения, скорость молокоотдачи и др. Имеются сведения о влиянии на заболеваемость коров маститами генотипа животных, в частности быков-производителей, их линейной принадлежности.
Большое значение имеют также исправность доильных установок, чистота доильно-молочного оборудования, соблюдение техники машинного доения коров, санитарное состояние помещений и прилегающих к ним территорий. мастит скот микроорганизм возбудитель
За последние годы достигнуты определенные успехи в области контроля над маститами. Разработаны и совершенствуются методы диагностики, особенно скрытых маститов. Широко применяются для лечения новейшие антимикробные препараты. Существующие методы и средства профилактики и лечения маститов не всегда дают ожидаемые результаты. Имеющийся опыт борьбы с маститами коров, основанный на проведении отдельных, часто разовых, мероприятий по диагностике, лечению и профилактике этой болезни показал их невысокую эффективность, поэтому в каждом хозяйстве необходима организация плановой системы мероприятий по борьбе с маститами коров.

КЛАССИФИКАЦИЯ МАСТИТА
По проявлению заболевания: клинический и скрытый (субклинический);
По течению болезни: острый, подострый, хронический;
По характеру воспаления (клинический): серозный, катаральный, гнойный, фибринозный, геморрагический, смешанные формы.
По обнаружению возбудителя:
• неспецифический – бактериальный, микозный, асептический;
• специфический – ящурный, актиномикозный, туберкулезный, бруцеллезный, оспенный, лептоспирозный.
Серозный мастит – ткани воспаленной доли пропитываются прозрачной жидкостью – серумом, выпотевающей из кровеносных и лимфатических сосудов.
Заболевание начинается с нарушений общего состояния: животные несколько угнетено, позыв на корм понижен, температура тела повышена, удой постепенно или резко снижается. Большая доля уплотнена, болезненна при ощупывании. Температура кожи этой доли, по сравнению с противоположной, повышена. Молоко из больной доли вымени более жидкое и в нем содержатся хлопья свернувшегося белка. При своевременно начатом лечении выздоровление наступает на третий день.
Катаральный мастит – чаще всего начинается с воспаления слизистой оболочки молочной цистерны и молочных ходов. Количество молока в воспаленной доле почти не уменьшается, но в нем содержатся комочки слипшихся белых кровяных клеток и кусочки отмершей слизистой оболочки. Общее состояние животного, как правило, не изменяется.
При распространении воспалительного процесса на железистую ткань количество молока уменьшается, в нем появляются хлопья и крошковидные сгустки. В отстоявшейся пробе молока виден слизисто-гнойный осадок. В пораженной доле у основания сосков прощупывается уплотнение величиной с грецкий орех. Если лечение начато своевременно, воспалительные явления затихают, однако продуктивность больной доли полностью не восстанавливается. При запоздалом или неполном курсе лечения заболевание принимает подострое или хроническое течение.
Фибринозный мастит – развивается как осложнение катарального мастита (при несвоевременном лечении последнего) и как самостоятельное заболевание при воспалительных процессах в половых органах и желудочно-кишечном тракте. Фибринозный мастит называется так потому, что в тканевой жидкости содержится белок крови – фибрин.
Заболевание характеризуется угнетенным состоянием, повышением температуры тела, болезненностью вымени, уменьшением или полным прекращением молокоотдачи. Вначале в молоке появляются фибринозные крошки, затем из соска пораженной доли с трудом выдаиваются несколько капель сыворотки с примесью гноя и фибринозных крошек. При прощупывании молочной цистерны у ее основания слышен хруст выпавшего фибрина, похожий на хруст снега. При осложнении фибринозного мастита развивается гангрена вымени. После выздоровления животного продуктивность пораженной доли полностью не восстанавливается.
Гнойный мастит – возникает при осложнении катаральных и фибринозных маститов. Заболевание протекает в острой и хронической формах. При остром течении болезни животное резко угнетено, температура тела достигает 41,5º С, коровы отказываются от корма. Пораженная доля вымени отечна, при ощупывании животное испытывает сильную боль, удои резко снижаются, а из пораженной доли выделяется сыворотка с примесью гноя.
При своевременно начатом лечении воспалительный процесс затухает и может перейти в хроническую форму. В результате больная доля постепенно уплотняется и перестает вырабатывать молоко.
Геморрагический мастит – как правило, развивается в первые дни лактации, поражает половину или все вымя, ткани пропитываются кровью, прошедшей через стенки кровеносных сосудов. Заболевание сопровождается ухудшением общего состояния животного, отеком и болезненностью вымени. Из пораженных долей вымени выдаивается небольшое количество красноватого водянистого молока, содержащего мелкие хлопья.
Флегмонозный мастит – разлитое гнойное воспаление подкожной клетчатки и интерстициальной ткани молочной железы. Развитию флегмоны обычно предшествуют открытые механические повреждения кожи и глубоко лежащих тканей с внедрением анаэробной микрофлоры. Флегмонозный процесс бурно развивается, охватывая всю долю или половину вымени. Кожа в очаге воспаления багрового цвета, глянцевитая вследствие отека, горячая, болезненная; хорошо заметны воспаленные лимфатические сосуды в виде тяжей, идущих к основанию вымени. Наружные паховые лимфатические узлы увеличены, болезненные. Из воспаленной доли с трудом удается получить несколько десятков миллилитров жидкого экссудата серого цвета. Пораженные ткани претерпевают некроз с образование язв и абсцессов; процесс может осложниться сепсисом.
Гангренозный мастит – осложняет другие формы мастита (серозный, фибринозный, геморрагический) в случае проникновения гнилостной (анаэробной) микрофлоры. При этом происходит распад продуктов воспалительного очага с выделением зловонных газов. Общее состояние животных крайне тяжелое. На коже пораженных долей вымени появляются плотные, болезненные, сине-красного или фиолетового цвета очаги в виде овальных возвышений. Соски приобретают сине-багровый или черный цвет. В дальнейшем происходит распад участков поражения с образованием гангренозных язв. Процесс нередко завершается сепсисом.
На территории Ярославской области лабораторные исследования болезней вымени коров и молока проводят специалисты отдела бактериологии ГБУ ЯО «Ярославская областная ветеринарная лаборатория».
Правила отбора и доставки проб молока (секрета вымени) в лабораторию.
Для микробиологического исследования отбирают пробы секрета из пораженных четвертей вымени или пробы молока из четвертей, реагирующих на быстрый маститный тест с соблюдением правил асептики. Перед взятием пробы молока соски вымени коров протирают ватным тампоном, смоченным 70 % раствором этилового спирта и выдаивают в конце дойки 5- 10 см3 молока в стерильные пробирки с пробкой. При взятии пробы сосок не должен касаться края пробирки.
Правила доставки проб молока (секрета вымени) в лабораторию.
Взятые пробы молока доставляют в лабораторию не позднее 4 часов с момента взятия в специальных емкостях, обеспечивающих температуру не выше 8- 10оС, или в термосах со льдом.
После исследования и установления возбудителя заболевания проводится определение чувствительности выделенных микроорганизмов к антибитикам диско-диффузионным методом.












